
Zestaw do analizy respirometrii organizmów wodnych
Zestaw Q-Box AQUA został zaprojektowany do pomiaru tempa metabolizmu (VO2) jako redukcji tlenu rozpuszczonego w komorze respirometrycznej z udziałem zwierząt wodnych. Przy pomocy tego systemu można badać zarówno kręgowce jak i bezkręgowce. Q-Box AQUA wykorzystuje zasadę respirometrii przepływowej. W jednym eksperymencie można monitorować do 4 komór, czyli do 4 próbek wodnych (przy użyciu odpowiednich komponentów). We wszystkich komorach panują takie same warunki eksperymentalne.
- Optyczna sonda tlenu
- Mała komora respirometryczna (140 ml, śr. wew. 3,8 cm, dł. 15,3 cm)
- Duża komora respirometryczna (660 ml, śr. wew. 8,2 cm, dł. 16,7 cm)
- Komora mini-AQUA (9 ml, śr. wew. 1,6 cm, dł. 4,5 cm)
- Mikrokomora (1,23 ml, śr. wew. 1,5 cm, gł. 0,85 cm)
- Sonda temperatury i zasolenia do kąpieli wodnej
- Pompa cieczy (1 l/min lub 0,1 l/min w mini-AQUA) i potrójny zawór
- Cyfrowa jednostka sterująca zaworem
- 6-kanałowy interfejs danych
- Oprogramowanie do zapisywania danych
- Czujnik ciśnienia bezwzględnego
- Wytrzymała, odporna na warunki atmosferyczne obudowa
Zastosowanie:
- Badania respirometryczne w środowisku wodnym
- Badania kręgowców i bezkręgowców wodnych
- Badania laboratoryjne i terenowe (z opcjonalną baterią)
Zasada działania systemu Q-Box AQUA
Zwierzę umieszcza się w komorze respirometrycznej, a następnie mierzy się spadek stężenia rozpuszczonego O2 spowodowany jego zużyciem. Dane dotyczące stężenia rozpuszczonego tlenu, skorygowane o zasolenie wody, temperaturę i ciśnienie, są wyświetlane w oprogramowaniu i wykorzystywane do obliczania bieżących wartości wskaźnika zużycia tlenu (VO2). Pomiary są wykonywane sekwencyjnie, bez wyjmowania zwierzęcia z komory. Komora jest przepłukiwana świeżą wodą pomiędzy pomiarami. Te przerywane pomiary przepływu VO2 eliminują wady ciągłej, zamkniętej respirometrii, w której poziom rozpuszczonego O2 w komorze może spaść do poziomu hipoksyjnego. Wszystkie elementy zestawu Q-Box AQUA są umieszczone w wytrzymałej, odpornej na warunki atmosferyczne obudowie, co ułatwia jego transport i przechowywanie.
Podczas eksperymentu woda krąży za pomocą pompy cieczy w komorze zwierzęcia i w naczyniu przepływowym z optyczną sondą tlenu. Główny zawór jest sterowany przez cyfrową jednostkę sterującą (DCU) oraz oprogramowanie, które definiuje czy system ma pracować w trybie cyrkulacji czy płukania. W trybie cyrkulacji wykonywane są pomiary oddychania, a w trybie płukania komora zwierzęca jest płukana wodą natlenioną z łaźni wodnej. Cykl cyrkulacji i płukania powtarzany jest aż do zakończenia eksperymentu. Czas płukania i fazy cyrkulacji wybierany jest przez użytkownika w oprogramowaniu.
Wersja mini-AQUA dla małych próbek
Do pomiarów respirometrii wodnej małych ryb i owadów (~1 g) Qubit oferuje zestaw mini-AQUA, który jest zmodyfikowaną wersję Q-Box AQUA. Mini-Aqua wyposażony jest w małą komorę wodną (9 ml) i komponenty do pomiaru mniejszej objętości całkowitej. Zestaw mini-AQUA zawiera również mikrokomorę (o objętości 1,23 ml) wraz z sondą do analizy rozpuszczonego tlenu. Wersja ta służy do pomiaru VO2 bardzo małych próbek, takich jak larwy i młode ryby o masie poniżej 0,5 g. Mikrokomora jest używana w trybie przerywanego przepływu, co zapewnia wyższą czułość pomiaru.

G223 mikro-komora systemu mini-AQUA
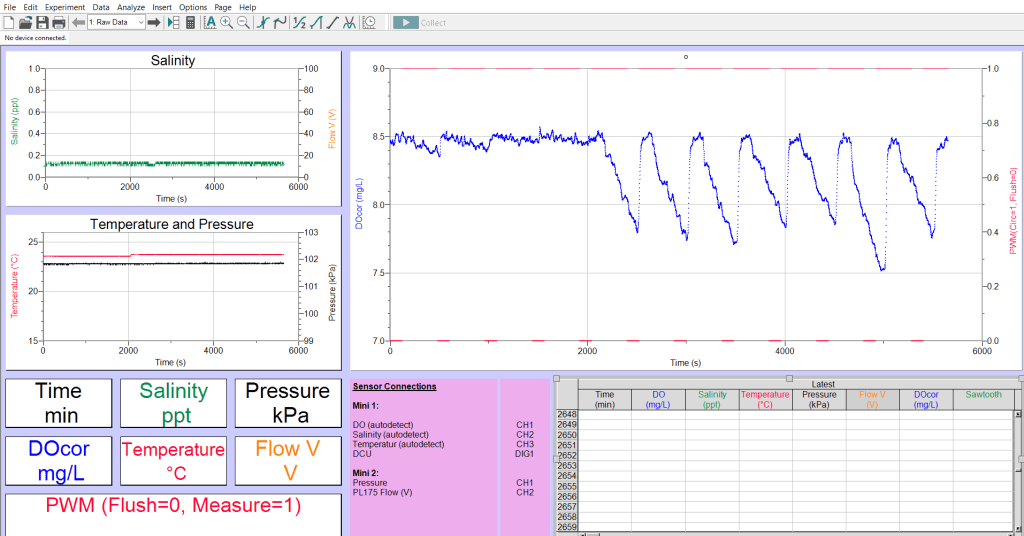
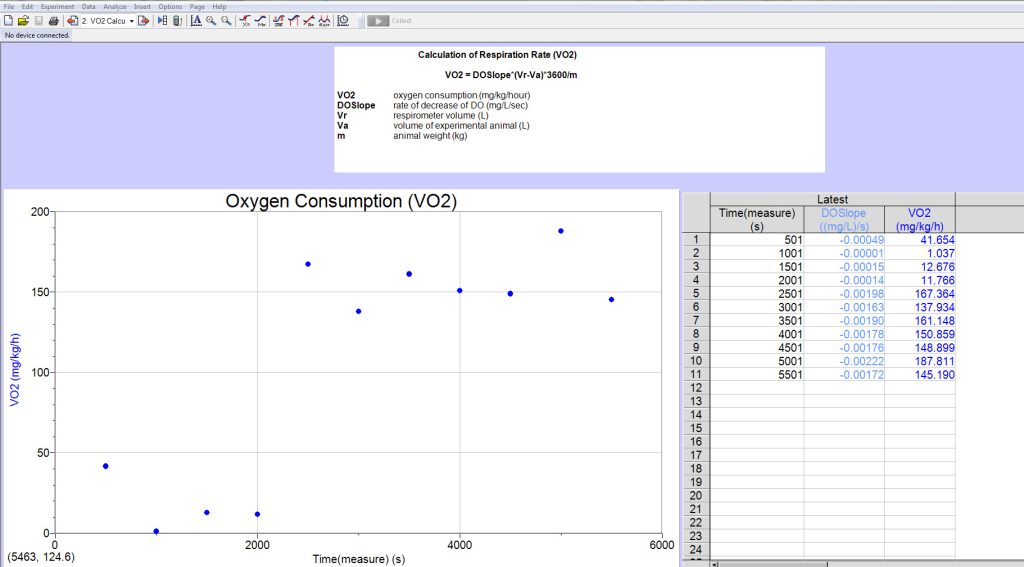
Oprogramowanie Q-Box AQUA
- G217 Duża komora oddechowa (śr. wew. 8,2 cm, dł. 16,7 cm, 660 ml)
- G216 Mała komora oddechowa (śr. wew. 3,8 cm, dł. 15,3 cm, 140 ml)
- G210 Komora mini-AQUA (śr. wew. 1,6 cm, dł. 4,5 cm, 9 ml)
- G223 Mikrokomora do mini-AQUA (śr. wew. 1,5 cm, gł. 0,85 cm, 1,23 ml)
- S122 Sonda optyczna do pomiaru tlenu
- A260 Naczynie przepływowe do sondy tlenu
- PL175 Pompa cieczy (1 l/min)
- PL100 Pompa cieczy (0,1 l/min) do mini-AQUA
- A236 Potrójny zawór
- C200 Cyfrowy moduł sterujący do zaworu potrójnego
- A750 Prosta plastikowa łaźnia wodna
- S132 Sonda temperaturowa do łaźni wodnej
- S181 Czujnik ciśnienia
- S130 Sonda zasolenia wody
- C610 6-kanałowy interfejs do zapisywania danych (x 2)
- C901 Oprogramowanie i C404 plik eksperymentalny
- Wytrzymała, odporna na warunki atmosferyczne obudowa
- Zestaw akcesoriów Q-Box AQUA przewody, złącza, filtry
- Instrukcja obsługi
- A249 zestaw baterii
M Aliende-Hernandez et al. (2024) Metabolic response of the starfish Coscinasterias Tenuispina (Lamarck, 1816) to ocean warming. Cah. Biol. Mar 65: 334-341
D H Hudson (2021) Metabolic response to temperature stress in the Colombian freshwater crab Neostrengeria macropa (H. Milne Edwards, 1853) (Decapoda: Brachyura: Pseudothelphusidae). Journal of Crustacean Biology, Feb 2021, 1-7 doi:10.1093/jcbiol/ruab002
Huang M et al. (2020) The Influence of Atrazine on the Growth, Development and Oxygen Consumption of Pelophylax nigromaculatus Tadpoles. Nature Environment and Pollution Technology 19: 1311-1317
Lamarre SG et al. (2019) Interrelationship between contractility, protein synthesis, and metabolism in mantle of juvenile Cuttlefish (Sepia officinalis). Frontiers in Physiology 10: 1051 doi: 10.3389/fphys.2019.01051
Keogh CL et al (2017) The double edge to parasite escape: invasive host is less infected but more infectable Ecology, 98(9) 2241–2247
Callaghan NI. Et al (2016) Zinc oxide nanoparticles trigger cardiorespiratory stress and reduce aerobic scope in the white sucker, Catostomus commersonii NanoImpact 2: 29–37
Lamarre SG. et al. (2016) Metabolic rate and rates of protein turnover in food deprived cuttlefish, Sepia Officinalis (Linnaeus1 1758). Am J Physiol Regul Intregr Comp Physiol 310: R1160-R1168
Bessemer RA. Et al. (2015) Cardiorespiratory toxicity of environmentally relevant zinc oxide nanoparticles in the freshwater fish Catostomus commersonii Nanotoxicology 9: 861-870SHAR

